Spinal Muscular Atrophy Treatments Available in Brazil / Tratamentos para Atrofia Muscular Espinhal (AME) disponíveis no Brasil
Drs Juliana Gurgel Giannetti and Rodrigo de Holanda Mendonça provide an overview of available treatments for spinal muscular atrophy in Brazil. / Drs Juliana Gurgel Giannetti and Rodrigo de Holanda Mendonça discutem tratamentos para atrofia muscular espinhal disponíveis no Brasil.
Episodes in this series

John Brandsema, MD: The new age that we have been in for about a decade, we initially had research trials and now clinical options for patients with SMA. There are 3 targeted therapies that have been approved in different care contexts around the world that are genetically targeted for SMA and make a significant difference in the experience of SMA for patients. Which treatments are available in Brazil for patients, and how do you decide about treatment selection in SMA? What factors should be taken into consideration in terms of patients and their clinical circumstances when deciding upon therapy?
Juliana Gurgel Giannetti, MD, PhD: I will address what is available in the Brazilian public health system. We have a public system that is universal, and according to the law, the government must provide treatment for everyone. We have the approval of the 3 SMA medications in Brazil by ANVISA [Brazilian Health Regulatory Agency]. Following the approval, the technical protocols are developed for use in the public health system. The technical protocols have approved 2 medications so far, nusinersen and risdiplam under certain criteria. The criteria for use via public health system are that pre-symptomatic patients can receive either nusinersen or risdiplam as long as they have up to 3 copies of the SMN2 gene. In symptomatic patients with SMA type 1, symptoms must have started before 6-months-old, patients must have up to 3 copies of SMN2 gene, and they cannot be on permanent invasive ventilation for more than 24 hours for more than 21 days. For patients with SMA type 2, the public health system protocol recommends the use of medication for patients aged between 2 years and 12 years who can sit and have good upper limb function. Patients aged older than 12 years have also recently been included under the same criteria. If the patient has severe scoliosis, many contractures, this will be a deterrent to using nusinersen, but they may have access to risdiplam. Risdiplam has not yet been approved for patients under 2-months-old—but it will be soon, and there may be some changes in protocol. These are the medications we can currently use according to the public health system in Brazil.
John Brandsema, MD: When we speak about these 3 treatments—nusinersen, onasemnogene abeparvovec, and risdiplam—we need to break down the differences between them and how we might monitor them clinically. Let´s start with Rodrigo, but the entire panel can contribute.
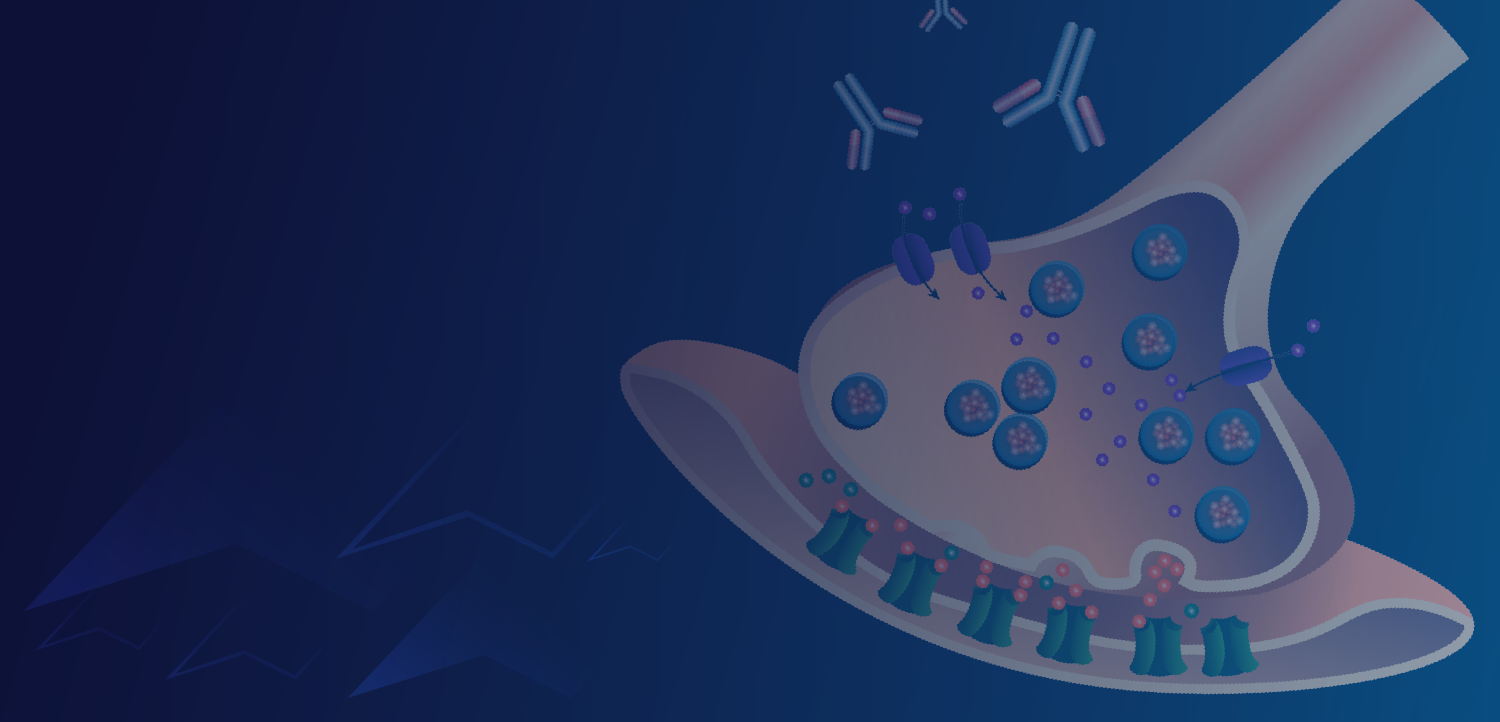
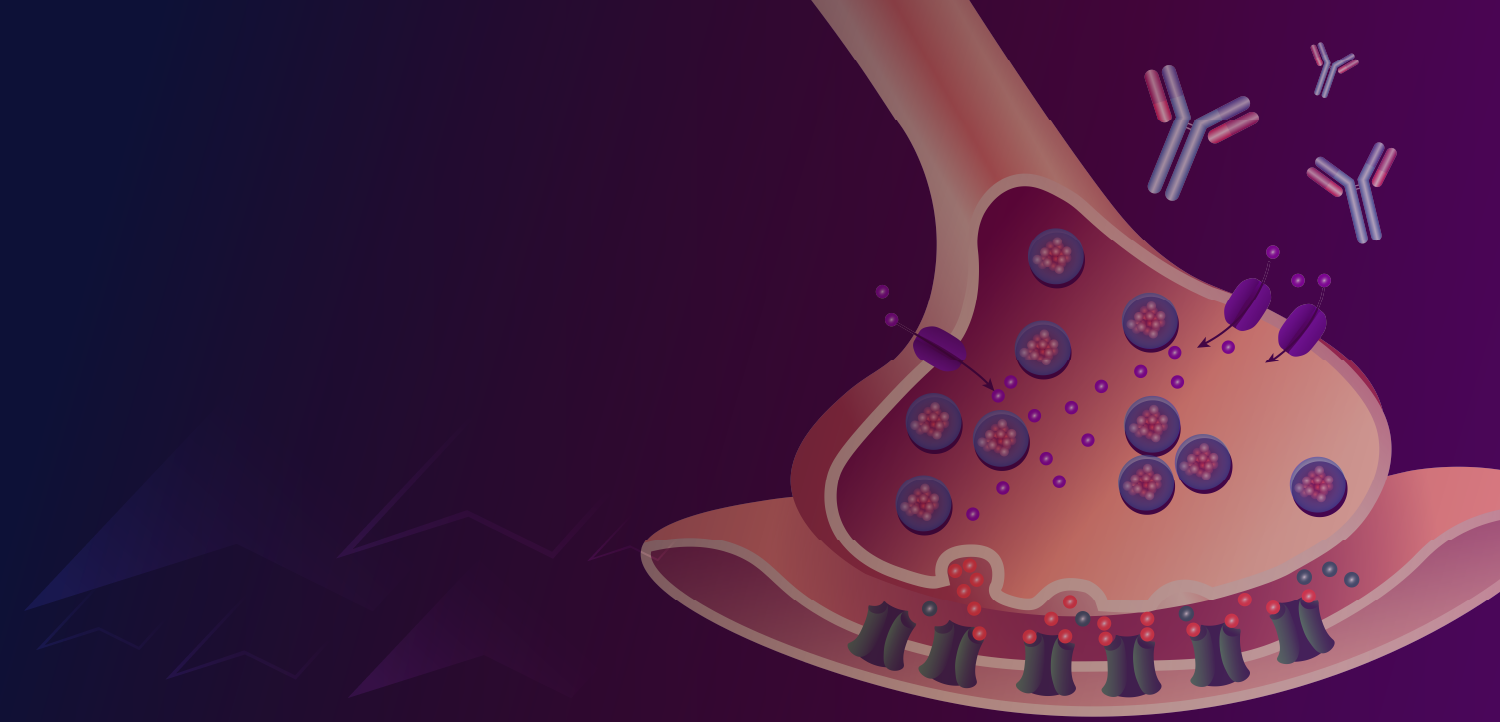
Rodrigo de Holanda Mendonça, MD:As Dr Giannetti said, we only have nusinersen and risdiplam available in the public health system, but ANVISA has approved the gene therapy onasemnogene abeparvovec. The first one that emerged was nusinersen in 2017, and it was the first approved treatment to change the natural history of SMA. It is an antisense oligonucleotide that acts by modulating the splicing of SMN2 gene. By modulating SMN2 splicing and increasing SMN protein levels, we stop the progressive degeneration of the motor neurons and can make motor improvement for patients with SMA. Since nusinersen is a large molecule, it does not cross the blood brain barrier, so it needs to be administered by an intrathecal route to reach the motor neuron. The dosage scheme consists of an attack dose and then maintenance doses throughout life, every 4 months. Nusinersen is a safe drug with no major adverse events—the main consideration is the intrathecal administration scheme. After nusinersen, 2 other therapies were approved by ANVISA. I will start with risdiplam because it has a mechanism of action similar to nusinersen, although it is a different molecule. Risdiplam is a small molecule that also modulates the splicing of SMN2, but it has the great advantage of being administered by daily oral doses according to the weight of the patient. Thus, it can be used in patients from birth to adulthood. Again, the level of SMN protein is expected to function in stopping the progressive death of motor neurons and promote motor improvements. The gene therapy onasemnogene abeparvovec was most recently approved by ANVISA and is currently under discussion for incorporation by the public health system. It has a different mechanism of action that is not focused on SMN2 but rather aims at replacing the SMN1 gene using a viral vector that carries the therapeutic gene—a copy of SMN1—to the motor neuron, the target cell. The patient then starts producing sustained levels of the SMN protein from this transfected SMN1 gene. The great advantage of gene therapy is that it can be administered intravenously in a single dose, and from then on, the patient is monitored and followed up by a specialist physician.
Transcript Edited for Clarity
Dr. John Brandsema: A nova era em que já estamos por cerca uma década, onde inicialmente tínhamos testes clínicos e hoje temos opções clínicas para pacientes com AME. Existem 3 terapias que foram aprovadas em diferentes contextos ao redor do mundo e que são geneticamente focadas na AME e fazem uma diferença significativa na experiência dos pacientes com AME. Quais tratamentos estão disponíveis para pacientes no Brasil e como você decide sobre a seleção do tratamento na AME? Quais fatores devem ser levados em consideração em termos do paciente e suas circunstâncias clínicas quando se decide uma terapia?
Dra. Juliana Gurgel Giannetti: Eu vou abordar o que está diponível no sistema público de saúde brasileiro. Nós temos um sistema público que é universal e, de acordo com a lei, o governo deve disponibilizar tratamento a todos. No Brasil, nós temos a aprovação das 3 medicações para AME pela ANVISA. A partir dessa aprovação, os protocolos técnicos para uso no sistema público de saúde são desenvolvidos. Os protocolos técnicos aprovaram 2 medicações por enquanto, nusinersena e risdiplam, com alguns critérios. Os critérios para uso via sistema público de saúde são que pacientes pré-sitnomáticos podem receber tanto nusinersena quanto risdiplam desde que tenham até 3 cópias do gene SMN2. Em pacientes sintomáticos com AME tipo 1, os sintomas devem ter iniciado antes dos 6 meses de vida, também devem ter até 3 cópias do gene SMN2, e eles não podem estar em ventilação invasiva permanente por mais de 24 horas por mais de 21 dias. Para pacientes com AME tipo 2, o protocolo do sistema público de saúde preconiza o uso da medicação para pacientes entre 2 e 12 anos com capacidade de sentar e que tenham boa função de membros superiores. Pacientes com mais de 12 anos também foram incluídos recentemente, sob os mesmos critérios. Se o paciente tiver escoliose grave, muitas contraturas, isso será um impeditivo ao uso de nusinersena, mas ele pode ter acesso ao risdiplam. O risdiplam ainda não foi aprovado para pacientes menores de 2 meses—mas está prestes a ser, então haverá algumas mudanças nesse protocolo. Essas são as medicações que podemos utilizar no Brasil, de acordo com o sistema público de saúde.
Dr. John Brandsema: Quando falamos desses 3 tratamentos—nusinersena, onasemnogeno abeparvoveque e risdiplam— precisamos explicar as diferenças entre eles e como os monitoramos na clínica. Vamos começar com o Dr. Mendonça, mas todos podem contribuir.
Dr. Rodrigo de Holanda Mendonça:Como a Dra. Giannetti falou, nós temos apenas nusinersena e risdiplam disponíveis no sistema público de saúde, mas a ANVISA já aprovou a terapia gênica onasemnogeno abeparvoveque. O primeiro que surgiu foi o nusinersena em 2017, e foi o primeiro tratamento para mudar a história natural da AME. Ele é um oligonucleotídeo antissenso que age modulando o splicing do gene SMN2. Modulando o splicing do SMN2 e aumentando os níveis da proteína SMN, nós paramos a degeneração progressiva dos motoneurônios e conseguimos possibilitar a melhora motora dos pacientes com AME. Como o nusinersena é uma molécula grande, ele não consegue atravessar a barreira hematoencefálica, então precisa ser administrado por via intratecal para chegar ao motoneurônio. O esquema de dosagem consiste de uma dose de ataque e doses de manutenção ao longo da vida, a cada 4 meses. Nusinersena é uma droga segura, sem grandes efeitos adversos—a maior consideração é a administração intratecal. Depois do nusinersena, 2 outras terapias foram aprovadas pela ANVISA. Vou começar com risdiplam porque ele tem um mecanismo de ação similar ao nusinersena, embora seja uma molécula diferente. O risdiplam é uma molécula pequena que também modula o splicing do gene SMN2, mas tem a grande vantagem de ser administrado por via oral, diária de acordo com o peso do paciente. Assim, pode ser usado em pacientes desde o nascimento até a idade adulta. Da mesma forma, espera-se que o aumento nos níveis da proteína SMN funcione em parar a morte progressiva dos motoneurônios e promova melhoras motoras. A terapia gênica onasemnogeno abeparvoveque foi recentemente aprovada pela ANVISA e está, no momento, sob discussão para incorparação no sistema público de saúde. Ela tem um mecanismo de ação diferente, que não é focado no gene SMN2, mas visa a reposição do gene SMN1 através de um vetor viral que carrega o gene terapêutico—uma cópia do SMN1—para o motoneurônio, a célula-alvo. O paciente, então, começa a produzir níveis sustentados da proteína SMN a partir to gene SMN1 transfectado. A grande vantagem da terapia gênica é que ela pode ser administrada por via intravenosa numa dose única, e partir disso, o paciente é monitorado e acompanhado por um especialista.
Transcrição editada para maior clareza
Newsletter
Keep your finger on the pulse of neurology—subscribe to NeurologyLive for expert interviews, new data, and breakthrough treatment updates.